联系方式
CONTACT INFO
检验科质控品选择与配置实操指南(附标准操作规程SOP)
检验结果的准确性是临床诊断和治疗的“生命线”,而质控品作为核心保障工具,能及时预警仪器故障、试剂失效、操作误差等风险,严防错误结果流入临床。然而,多数检验科在质控品选择与配置中常遇诸多困惑:多水平与单水平该如何抉择?冻干品复溶有哪些关键要点?不同检测项目质控品能否混用?本文将从“科学选择”“精准配置”两大核心环节拆解实操要点,并附标准操作规程(SOP),助力规避90%以上的常见问题。
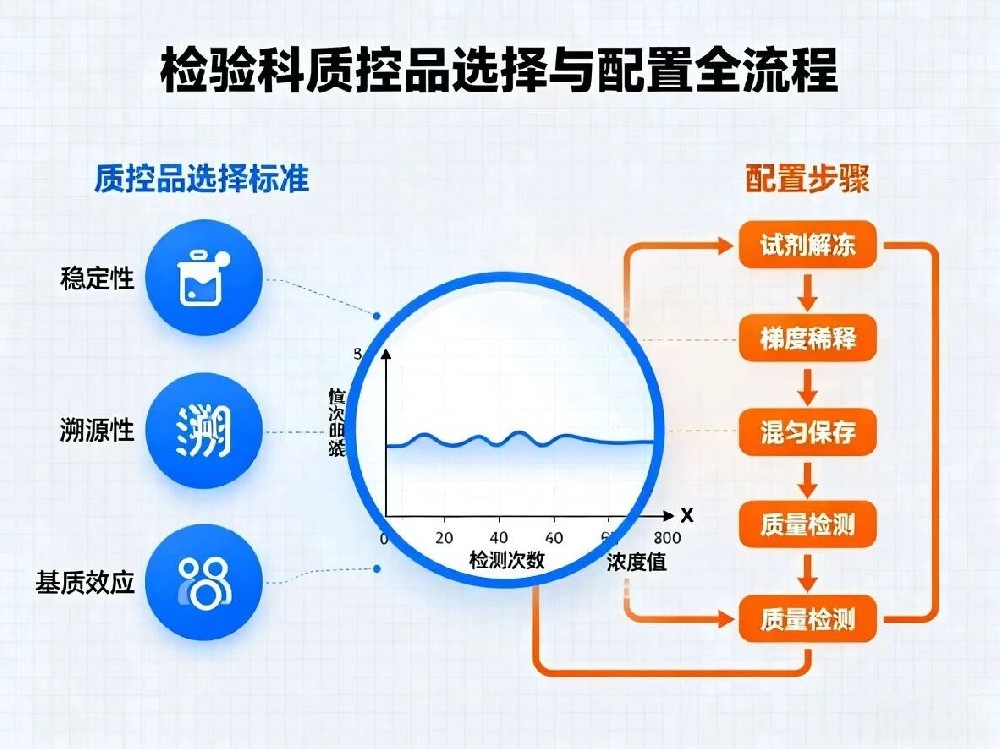
一、质控品科学选择:4大核心维度精准定位
质控品的选择是质控工作的基础,若选择不当,后续操作再精准也会功亏一篑。需重点把控以下4个核心维度:
1. 项目精准匹配:严格遵循“专品专用”原则
质控品必须与实验室检测项目、检测方法及仪器类型完全适配,严禁跨界通用。不同检测领域的质控品因检测目标、基质成分差异显著,混用会导致结果严重偏差:
生化项目(如肝功能、血糖、血脂):质控品核心成分为酶、代谢物等,基质多为血清或血浆;
免疫项目(如乙肝五项、肿瘤标志物、甲状腺功能):需含特异性抗原/抗体,基质常经过特殊处理以模拟临床样本免疫特性;
分子诊断项目(如新冠核酸、HPV检测、耐药基因检测):需含特定靶核酸片段,且需匹配检测仪器的荧光通道、扩增体系等关键参数。
2. 质量合规性:认准权威认证,杜绝“三无产品”
质控品质量直接决定质控结果的可靠性,需同时满足国家标准(GB/T相关系列)和国际标准(ISO 15189相关要求),并具备权威机构出具的资质证明:
优先选择持有《标准物质证书》(有证标准物质,CRM)或《校准与测量能力证书》(CMC证书)的产品;
严格核查生产资质(医疗器械生产许可证)、产品批号、完整说明书等关键信息,坚决杜绝无资质、无批号、无说明书的“三无产品”,避免因成分不稳定、靶值不准导致“假失控”或“假在控”。
3. 规格适配性:按需选择水平与用量
需结合检测项目的临床意义和实验室日均检测量,精准匹配质控品规格:
水平选择:需覆盖临床常见结果区间,常规项目(血常规、基础生化)选择2个水平(正常参考值水平+临界值水平);特殊项目(凝血功能、毒理学检测、激素检测)需选择3个水平(正常+临界+异常),确保全区间质控覆盖。
用量选择:结合日均检测量和开封后稳定期综合判断。日均检测量≤100份的项目,优先选小规格(如200μL/支、500μL/支),避免开封后反复冻融导致成分降解;日均检测量≥500份的项目,可选大规格(如1mL/支、2mL/支),减少批号更换频率,降低系统误差。
4. 稳定性把控:规避临期品,算清“使用窗口期”
稳定性是质控品的核心属性,需重点关注储存条件和有效期限:
核查说明书明确的储存条件(如-20℃冷冻、2-8℃冷藏、室温保存),确保实验室储存环境达标;
标注“未开封有效期”和“开封后稳定期”,如未开封-20℃保存有效期1年,开封后2-8℃保存稳定7天,需严格在稳定期内使用;
规避临期产品(距有效期不足3个月),尤其冻干质控品,临期可能出现成分微量降解,导致靶值漂移。
二、质控品精准配置:3步标准流程实现“零误差”
配置环节的细节误差是质控失控的“隐形杀手”。以临床最常用的冻干型质控品(需复溶)为例,标准操作流程如下:
1. 配置前核查:3项关键检查杜绝先天隐患
配置前需完成外观、信息、溶剂三项核查,排除不合格产品:
外观核查:冻干质控品应为均匀疏松粉末,无结块、变色、吸潮现象;液体质控品应澄清透明,无浑浊、沉淀、分层、变色。若出现异常,立即报废,严禁使用。
信息核查:核对质控品名称、批号、有效期,确保与检测项目的试剂批号匹配(部分项目如凝血、免疫需同批号试剂对应同批号质控品),记录批号信息便于追溯。
溶剂核查:必须使用产品自带专用溶剂或说明书指定溶剂(如无酶纯水、专用缓冲液),严禁用自来水、普通生理盐水替代,避免引入杂质或改变基质环境。
2. 配置中操作:精准把控3个核心要点
加样精准化:使用经计量校准的移液枪(校准周期≤6个月),按说明书要求精准加样,如1支冻干质控品加0.5mL溶剂,误差控制在±1%以内。加样过多会导致浓度偏低,加样过少会导致浓度偏高,直接影响质控结果。
复溶充分化:加溶剂后,轻轻颠倒离心管3-5次(避免剧烈震荡产生气泡),室温静置5-15分钟(具体时间参照说明书),确保粉末完全溶解,无肉眼可见颗粒。未溶解颗粒会堵塞仪器管路,还会导致检测结果偏低。
混匀适度化:复溶后轻轻混匀3-5次,避免反复抽打或剧烈震荡,防止蛋白质变性(尤其免疫类质控品)或核酸降解(分子类质控品),确保成分均匀分布。
3. 配置后处理:2个关键动作保障稳定性
及时分装储存:复溶后若单次用不完,按单次用量分装至无菌离心管,清晰标注“质控品名称+批号+复溶日期+失效日期”,1小时内放入-20℃冷冻保存,且仅限冻融1次(反复冻融会破坏成分稳定性)。
同步校准验证:新配置质控品首次使用前,需与标准品或前一批次合格质控品进行比对,验证靶值和标准差(SD)是否在允许范围内(偏差≤5%)。若偏差超标,需重新核查配置步骤(如加样量、复溶时间),排除误差后再使用。
三、避坑指南:3大常见误区深度解析
误区1:不同批号质控品混用
不同批号质控品的靶值、标准差(SD)存在固有差异,混用会导致质控数据无法追溯,一旦出现失控,无法区分是仪器故障、试剂问题还是质控品本身的差异,严重影响问题排查的准确性。正确做法:同一检测项目同时间段内使用同一批号质控品,批号更换时需重新确定靶值和SD,并记录更换时间。
误区2:复溶后室温放置过久
复溶后的质控品稳定性显著下降,室温放置时间过长会导致成分降解(如酶活性降低、抗原抗体结合能力下降、核酸降解),引发结果漂移。正确做法:复溶后30分钟内完成检测,敏感项目(如凝血质控品、激素质控品)需在15分钟内完成,严格执行“现配现用”原则。
误区3:忽视储存条件要求
未按说明书要求储存是导致质控品提前失效的主要原因,如将需-20℃冷冻保存的质控品长期放置于2-8℃冰箱,会导致成分缓慢降解,即使在有效期内也会出现“假失控”。正确做法:冰箱张贴储存条件标识,定期监测并记录储存温度(每日至少2次),不同储存条件的质控品分区存放,避免交叉污染。
四、检验科质控品选择与配置标准操作规程(SOP)


1. 目的
规范检验科质控品的选择、采购、验收、配置、储存及使用流程,确保质控结果准确可靠,保障检验质量。
2. 适用范围
本规程适用于检验科所有检测项目(生化、免疫、分子诊断、凝血、血常规等)的质控品管理。
3. 职责分工
检验科负责人:审批质控品采购计划,监督规程执行;
质量负责人:审核质控品资质,定期核查质控品管理情况;
检验技师:执行质控品选择建议、配置、使用及记录工作。
4. 操作流程及要求
4.1 质控品选择与采购
根据检测项目、仪器型号、检测方法,按“项目匹配、质量合规、规格适配、稳定性优先”4大维度筛选候选产品;
索要候选产品的生产资质、标准物质证书、说明书等资料,由质量负责人审核;
制定采购计划,经检验科负责人审批后采购,采购时明确批号、有效期(距失效期≥6个月)。
4.2 质控品验收
到货后核查外包装是否完好,无破损、渗漏;
核对产品名称、批号、有效期、规格与采购计划一致;
抽样检查外观(冻干品无结块、液体品无浑浊),符合要求后方可入库,填写《质控品验收记录》。
4.3 质控品储存
按说明书要求分区储存(-20℃冷冻区、2-8℃冷藏区、室温区),张贴明显标识;
每日监测并记录储存温度,温度异常时及时转移至备用设备,排查原因;
遵循“先进先出”原则,临近有效期的质控品优先使用。
4.4 质控品配置(冻干型)
配置前准备:消毒操作台,准备经校准的移液枪、专用溶剂、无菌离心管;
外观与信息核查:确认质控品无异常,批号与试剂匹配;
精准加样:按说明书加溶剂,误差≤±1%;
复溶与混匀:轻轻颠倒后室温静置5-15分钟,确保完全溶解,适度混匀;
分装与储存:单次用不完的按单次用量分装,标注信息后冷冻保存;
校准验证:首次使用前与标准品比对,偏差≤5%方可使用,填写《质控品配置记录》。
4.5 质控品使用与追溯
每次使用前核查批号、失效期,确认储存条件合格;
严格按“现配现用”原则,复溶后30分钟内完成检测;
记录质控结果、质控品批号、使用日期等信息,确保全程可追溯;
批号更换时重新确定靶值和SD,记录更换原因及时间。
4.6 不合格质控品处理
外观异常、过期、校准不合格的质控品,标注“不合格”标识,按医疗废弃物处理规定销毁,填写《不合格质控品处理记录》。
5. 记录与存档
《质控品验收记录》《质控品配置记录》《质控品储存温度记录》《不合格质控品处理记录》等资料,存档期限≥3年。
6. 附则
本规程由检验科负责解释,每年根据最新标准及实验室实际情况修订一次。
五、结语
质控无小事,细节定成败。质控品的选择与配置作为检验质量控制的核心环节,直接关系到临床诊断的准确性和患者的诊疗安全。唯有严格遵循科学选择标准、执行精准配置流程、规避常见误区,才能让质控工作真正发挥“预警器”和“守护者”的作用。
若实验室在特殊项目(如罕见病检测、新型分子诊断项目)的质控品管理中存在困惑,可结合项目特性进一步细化SOP,或咨询专业质控品生产厂家的技术支持。
- 上一篇:医学检验中质控品与校准品的核心差异
- 下一篇:质控品的正确选择方法

